นิยามของออสโมซิส
ออสโมซิสคือทางเดินที่เกิดขึ้นเองของตัวทำละลาย (ซึ่งในระบบชีวภาพมักจะเป็นน้ำ) จากการแก้ปัญหาที่ตัวละลายถูกเจือจางมากกว่าตัวทำละลายที่เข้มข้นขึ้น การเคลื่อนไหวนี้ - ซึ่งเกิดขึ้นผ่านเยื่อหุ้มเซลล์แบบ semipermeable - จะดำเนินต่อไปจนกว่าจะถึงสภาวะสมดุลซึ่งทั้งสองวิธีจะได้รับและรักษาความเข้มข้นเดียวกัน
ตัวอย่างการปฏิบัติ
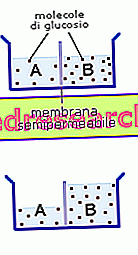
เพื่อให้แนวคิดของออสโมซิสชัดเจนยิ่งขึ้นเราจินตนาการว่าการมีเรือแบ่งออกเป็นสองส่วนที่มีปริมาตรเท่ากัน (A และ B) โดยเยื่อหุ้มเซลล์แบบกึ่งสังเคราะห์ (เช่นดูดซึมได้เฉพาะกับตัวทำละลาย - ในกรณีนี้น้ำ - และไม่ใช่ตัวถูกละลาย) ในห้อง A มีสารละลายน้ำที่น้ำตาลกลูโคสหนึ่งช้อนถูกละลายในขณะที่ในส่วน B เรามีสารละลายที่มีปริมาตรเท่ากันซึ่งน้ำตาลกลูโคส 3 ช้อนโต๊ะละลาย (มันเข้มข้นมากกว่า) ความแตกต่างนี้สร้างการไล่ระดับความเข้มข้นสำหรับน้ำตาลกลูโคสที่ด้านข้างของเยื่อหุ้มเซลล์และเนื่องจากน้ำตาลชนิดนี้ไม่สามารถผ่านได้ความสมดุลจึงมาถึงเมื่อน้ำผ่านจากห้อง A (ซึ่งกลูโคสเจือจางมากขึ้น) ไปที่ห้อง B (มันมีมากขึ้น) หากคุณต้องการคุณยังสามารถพูดได้ว่าน้ำที่ผ่านการออสโมซิสจากการแก้ปัญหาที่มีความเข้มข้นมากขึ้น (A) ไปที่สิ่งที่มันอยู่ในวัดที่เล็กกว่า (B)
หลังจากการไหลนี้ระดับน้ำใน B เพิ่มขึ้นและลดลงใน A ทำให้เกิดความแตกต่างในระดับระหว่างสองระดับ ปรากฏการณ์นี้สิ้นสุดลงเมื่อสารละลายทั้งสองมีความเข้มข้นเท่ากันทำให้คงที่
โซลูชัน Hypotonic, isotonic และ hypertonic
ด้วยการแก้ปัญหาทั้งสองด้วยความเข้มข้นของฟันกรามที่แตกต่างกัน (จำนวนของอนุภาคที่ละลายในพวกเขาที่แตกต่างกัน) วิธีการแก้ปัญหาที่มีความเข้มข้นของฟันกรามและ hypertonic ที่ต่ำกว่าคือเข้มข้นที่สุด วิธีแก้ปัญหาสองวิธีนั้นแทน isotonic (หรือ equimolar) เมื่อพวกเขามีความเข้มข้นเดียวกัน
ในตัวอย่างที่เพิ่งเสร็จสิ้นการแก้ปัญหา B คือ hypertonic (ดังนั้นจึงมีตัวถูกละลายมากขึ้น) กว่าอื่น ๆ (กำหนดเป็น hypotonic); ดังนั้นภายใต้สภาวะปกติตัวทำละลายจะย้ายโดยออสโมซิสจากไฮโปโทนิกไปยังสารละลายไฮโตรนิก เราพูดคุยเกี่ยวกับเงื่อนไขมาตรฐานเพราะโดยการเล่นกับกฎของฟิสิกส์มันเป็นไปได้ที่จะคว่ำแนวคิดของออสโมซิสและสนับสนุนทางเดินของตัวทำละลายจากความเข้มข้นที่เจือจางมากขึ้นถึงความเข้มข้นที่มากขึ้น (ออสโมซิย้อนกลับ)
แรงดันออสโมติกและรีเวิร์สออสโมซิส
เท่าที่แสดงจนถึงขณะนี้กระแสสุทธิของตัวทำละลาย - ที่เกิดจากการออสโมซิส - ยังคงดำเนินต่อไปจนกว่าทั้งสองโซลูชั่นจะมีความเข้มข้นเท่ากัน การเคลื่อนไหวนี้สามารถตอบโต้หยุดหรือย้อนกลับได้โดยใช้แรงกดกับช่องที่มีความเข้มข้นสูงสุด

ในตัวอย่างก่อนหน้านี้มันเพียงพอที่จะวางลูกสูบในห้อง B (ซึ่งเราจำได้ว่ามีความเข้มข้นสูงกว่า) และดันมันลงด้วยแรงบางอย่างเพื่อสนับสนุนทางน้ำไปยัง A; ในกรณีนี้เราพูดถึงการ Reverse Osmosis
แรงดันออสโมติกคือความดันที่ต่อต้านการผ่านของตัวทำละลายผ่านเยื่อหุ้มเซลล์แบบกึ่งสังเคราะห์; ผลที่ตามมาก็คือแรงกดดันที่จำเป็นในการต่อสู้กับการดูดซึม
ดังที่ได้กล่าวมาแล้วสองวิธีแก้ปัญหาไอโซโทปโม้ความดันออสโมติกเดียวกัน เพื่อขีดเส้นใต้ดังนั้นแรงดันออสโมติกจึงขึ้นอยู่กับจำนวนของอนุภาคที่มีอยู่ในสารละลายและไม่ขึ้นกับธรรมชาติ
ออสโมซิสและร่างกายมนุษย์
พลาสมาเมมเบรนที่ล้อมรอบเซลล์ของร่างกายมนุษย์ในความเป็นจริงคือเยื่อกึ่งดูดซึมได้ซึ่งอนุญาตให้ผ่านโดยตรงโดยการออสโมซิสของโมเลกุลขนาดเล็ก (เช่นน้ำและยูเรีย) แต่ไม่ใช่พวกที่มีน้ำหนักโมเลกุลสูงกว่า (เช่น โปรตีนกรดอะมิโนและน้ำตาล) สมดุลออสโมติกในของเหลวในร่างกายจึงเป็นสิ่งจำเป็นเพื่อให้แน่ใจว่าเซลล์มีสภาพแวดล้อมที่ดีที่สุดที่จะมีชีวิตอยู่
ถ้าเราเอาเซลล์เหมือนเซลล์เม็ดเลือดแดงแล้วจุ่มลงในสารละลายไฮโปโทนิกสิ่งนี้ - โดยการออสโมซิส - จะมีอาการบวม (ที่ได้รับจากทางน้ำ) ซึ่งสามารถทำให้เกิดการระเบิดได้ ในทางตรงกันข้ามถ้าแช่อยู่ในสารละลายไฮโตโตนิกเซลล์จะผ่านเนื่องจากน้ำไหลไปทางด้านนอกทำให้เกิดการขาดน้ำอย่างรุนแรงซึ่งทำให้เซลล์เหี่ยวเฉา โชคดีที่ในสิ่งมีชีวิตมนุษย์เซลล์ถูกแช่อยู่ในสารละลายไอโซโทนิกเกี่ยวกับสภาพแวดล้อมภายในและมีระบบต่าง ๆ ที่จะทำให้ของเหลวเหล่านี้อยู่ในสภาวะสมดุลออสโมติก
แรงดันออสโมติกและการถนอมอาหาร
เราคิดว่าครู่หนึ่งเกี่ยวกับแยมโฮมเมด ... น้ำตาลถูกเติมเข้ามาอย่างมากมายไม่เพียง แต่จะช่วยเพิ่มรสชาติ แต่ยังรวมถึงสิ่งอื่น ๆ เพื่อเพิ่มอายุการเก็บรักษา แต่น้ำตาลเป็นองค์ประกอบที่สำคัญสำหรับชีวิตของจุลินทรีย์จำนวนมากที่เกี่ยวข้องกับการย่อยสลายของผลิตภัณฑ์ ความแตกต่างที่เห็นได้ชัดนี้ถูกถอดออกโดยแนวคิดของออสโมซิส